近日,南开大学生命科学学院生物活性材料教育部重点实验室孔德领教授课题组的王恺副研究员和丁丹教授团队在Advanced Materials期刊(IF:30.849)发表了题为“Highly Bright AIE Nanoparticles by Regulating the Substituent of Rhodanine for Precise Early Detection of Atherosclerosis and Drug Screening”的研究论文。该研究制备了一种高亮度聚集诱导发光(AIE)纳米探针,这种纳米探针能够特异性结合在动脉粥样硬化(AS)斑块中过表达的CD47分子,可以精确、灵敏地识别载脂蛋白E缺陷(ApoE-/-)小鼠不同阶段的AS斑块,并可用于快速筛选抗AS药物(图1)。
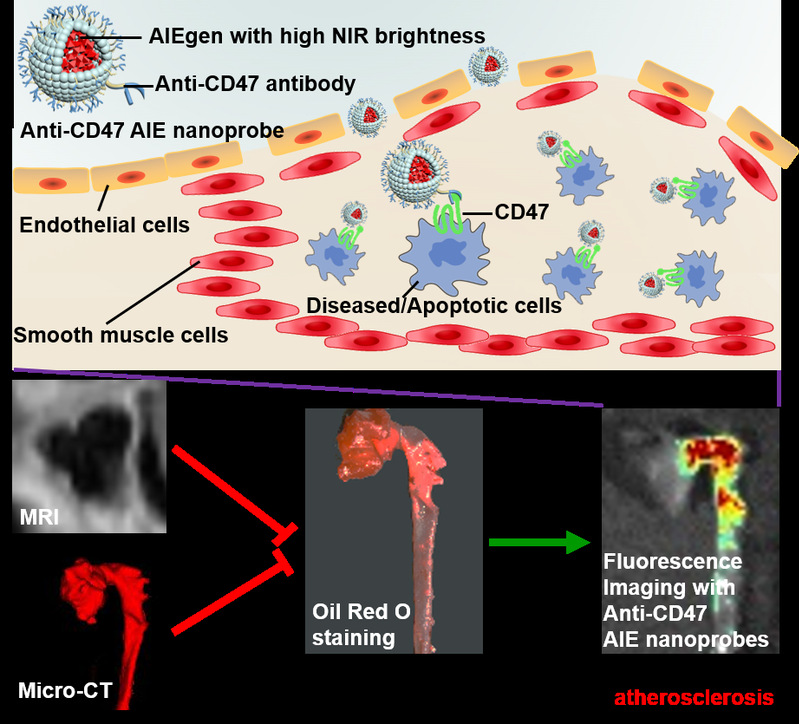
图1 AIE纳米探针靶向早期动脉粥样硬化斑块示意图
AS以数十年无症状的斑块积聚为特征,严重时会导致致命性心血管事件的突然发生,包括斑块破裂、心肌梗死、卒中,甚至猝死。因此,早期准确地检测AS,结合尽早地主动治疗,对降低危及生命的心血管事件的发生率至关重要。目前临床上采用X射线CT(X-ray computed tomography, CT)和磁共振成像(magnetic resonance imaging, MRI)对AS进行无创检测,然而,这些成像技术仅能识别晚期AS斑块,迫切需要开发先进的成像技术来检测早期AS斑块。
该研究制备的纳米探针以两亲性共聚物为基质封装TPE-T-RCN分子,并在其表面进一步功能化抗CD47抗体,以特异性结合AS斑块中过表达的CD47分子。当静脉注射动脉粥样硬化小鼠后,靶向纳米探针可以特异性聚集在斑块区域,从而实现Micro-CT和MRI所无法完成的早期斑块检测。AS是一种进行性疾病,在治疗与监控过程中,往往需要多次检测,我们的数据显示多次注射该纳米荧光探针也不会对AS疾病进程造成影响。此外,以抗AS药物阿托伐他汀(AT)和肝脏X受体激动剂GW3965(GW)为例,基于该荧光纳米颗粒还可实现先于MRI和Micro-CT的抗AS药物疗效的快速筛查,有益于加快抗AS药物的研发进度(图2)。
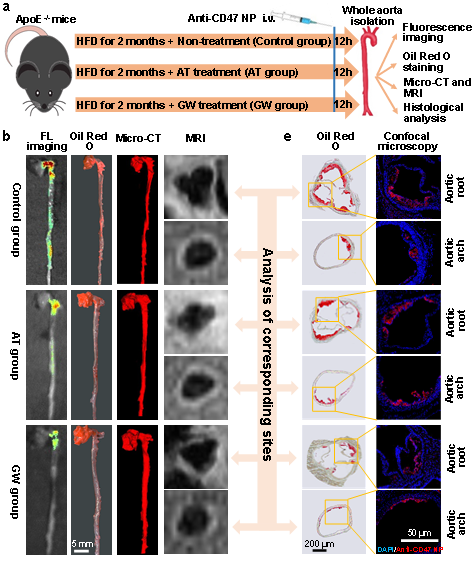
图2 抗CD47纳米探针用于检测早期AS和监测抗AS药物功效
此外,该研究通过荧光成像以及组织切片分析进一步验证了抗CD47纳米探针能够准确靶向人颈动脉斑块(图3)。
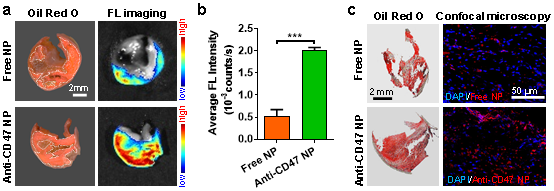
图3 抗CD47纳米探针与人颈动脉斑块的靶向结合
该论文由南开大学生命科学学院王恺副研究员与博士后高贺麒为共同第一作者,南开大学生命科学学院丁丹教授为本论文的共同通讯作者。本研究得到了创新研究群体项目(81921004),国家自然科学基金项目(51961160730)等的支持。
论文链接:https://doi.org/10.1002/adma.202106994.



