心力衰竭是一种严重威胁生命的疾病,被称为“生命绊脚石”。任何会引起心脏结构及功能异常的因素均会导致心力衰竭,如年龄、冠心病、高血压、瓣膜性心脏病、左心室肥大、糖尿病和肥胖等,长期的高胆固醇血症与动脉粥样硬化是导致心力衰竭发生与发展最重要的因素之一。迄今为止,治疗心力衰竭的药物主要有利尿剂、他汀类药物以及血管紧张素受体、β-受体和钙通道阻滞剂等,但疗效有限,因而,心力衰竭仍然是全球死亡的主要原因之一。相应的基础研究进展缓慢,其中一个重要原因是缺乏合适的动物模型,因此,发展新的动物模型和潜在药物迫在眉睫。
韩际宏教授研究组采用载脂蛋白E(ApoE)和低密度脂蛋白受体(LDLR)双基因缺陷(ApoE-/-LDLR-/-)小鼠构建了高胆固醇血症/动脉粥样硬化诱导的心力衰竭新模型,在HFD喂养下,ApoE-/-LDLR-/-小鼠不仅会发生高胆固醇血症和动脉粥样硬化,还会发生冠状动脉病变进而导致心力衰竭。经16周的高脂喂食后,作者观察到了心脏损伤/衰竭的典型特征,表明他们成功构建了高胆固醇血症/动脉粥样硬化导致心力衰竭的新模型。
基于新模型,并结合网络药理学、转录组测序及分子生物学等技术,研究了复方丹参滴丸(CDDP)或CDDP联合低剂量辛伐他汀对心力衰竭的治疗作用及机制,该研究成果“Compound Danshen Dripping Pill inhibits hypercholesterolemia/atherosclerosis-induced heart failure in ApoE and LDLR dual deficient mice via multiple mechanisms”近日在线发表于国际知名期刊Acta Pharmaceutica Sinica B。

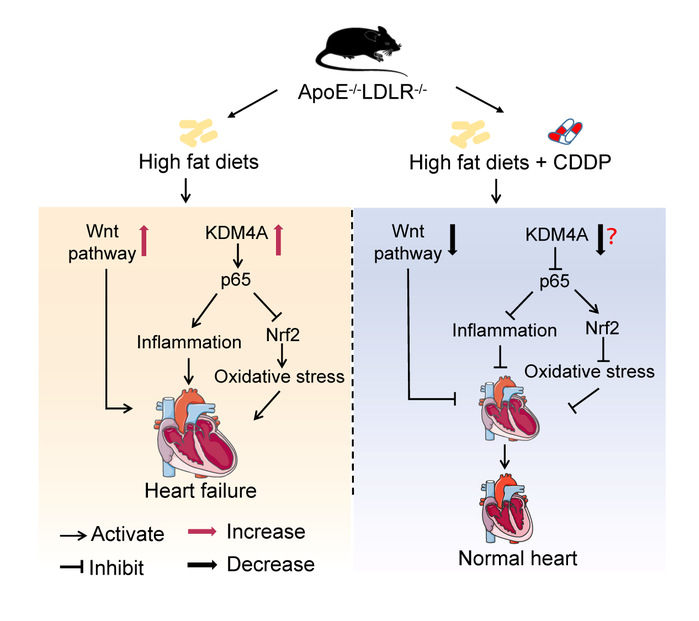
该研究组发现,在心衰后,Wnt通路和赖氨酸特异性去甲基化酶4A(KDM4A)在心脏损伤小鼠中均被显著激活。相反,CDDP或CDDP联合低剂量的辛伐他汀能够显著上调Wnt通路抑制因子的表达从而抑制Wnt通路。同时,CDDP通过抑制KDM4A的表达和活性来实现抗炎和抗氧化应激作用。此外,CDDP改善了辛伐他汀诱导的骨骼肌肌溶解。综上所述,该研究表明,CDDP单独或联合低剂量辛伐他汀可以通过多种作用机制抑制心脏损伤,从而有效改善高胆固醇血症/动脉粥样硬化引起的心力衰竭,这些研究结果可为临床应用提供理论基础。
南开大学生命科学学院博士生杨艳芳、博士毕业生冯科为本文共同第一作者。南开大学生命科学学院韩际宏教授,天士力星斗云创新研发技术平台负责人胡蕴慧博士,中国科学技术大学附属第一医院段亚君教授为本文通讯作者。该项目得到国家自然科学基金、天津市科学技术委员会和中央高校基本科研业务费专项资金的支持。
(论文链接:https://doi.org/10.1016/j.apsb.2022.11.012)
此外,近期韩际宏教授等人受主编邀请在Signal Transduction and Targeted Therapy期刊发表题为“Regulation of cholesterol homeostasis in health and diseases: from mechanisms to targeted therapeutics”综述文章。该文首先回顾了胆固醇研究的历史和重要里程碑事件,继而总结了胆固醇稳态的重要调控机制、临床或临床前研究中的针对胆固醇水平的干预措施、以及新的降胆固醇靶点,最后详细讨论了针对胆固醇稳态的药物干预对治疗多种疾病的益处,包括动脉粥样硬化性心血管疾病、肥胖、糖尿病、非酒精性脂肪肝、癌症、神经退行性疾病、骨质疏松症和病毒感染,有助于加深研究人员对胆固醇稳态和干预措施的深入理解。
(论文链接:https://www.nature.com/articles/s41392-022-01125-5)



