β-Arrestins (βarrs)介导活化的G蛋白偶联受体(GPCRs)的脱敏和内化。二聚的C家族GPCR成员募集抑制蛋白的分子机制仍然不清楚。

2025年3月5日,南开大学杨雪、沈月全共同通讯在Nature Chemical Biology(IF=13) 在线发表题为“Molecular basis of β-arrestin coupling to the metabotropic glutamate receptor mGlu3”的研究论文,该研究揭示了β-Arrestins与代谢型谷氨酸受体mGlu3偶联的分子基础。
GPCRs在感知细胞外信号和调节许多生理过程中起着关键作用。配体结合的GPCRs选择性激活G蛋白或抑制蛋白途径的偏向性信号转导现象,对于开发更具靶向性且副作用更少的药物具有重要的治疗潜力。β-抑制蛋白(βarr1和βarr2)是GPCR活性调节的核心,促进受体脱敏、内化和信号传导。这些支架蛋白被磷酸化的GPCRs募集,这是一种由GPCR激酶(GRKs)促进的翻译后修饰。先前的研究揭示了GPCRs和抑制蛋白之间的两种不同的相互作用模式:核心构象和尾部构象。前者涉及受体的跨膜核心和磷酸化尾部与抑制蛋白的全面结合,如抑制蛋白与几个A GPCRs S11–16家族的相互作用所示。后者涉及磷酸化尾单独或与受体的其他部分结合。在βarr1与家族B GPCR(胰高血糖素受体(GCGR)17)偶联的最新结构中,磷酸化尾和螺旋VIII都有助于相互作用。尾巴构象的功能性以前已有报道。
代谢型谷氨酸受体(mGlus)调节中枢神经系统中的突触传递。在家族C GPCRs下分类,mGlu亚组包含8个不同的亚型(mGlu1至mGlu8)。mGlus作为专性同源或异源二聚体发挥功能,每个原聚体由一个捕蝇草(VFT)结构域、一个富含半胱氨酸的结构域(CRD)和一个七跨膜结构域(7-TMD)组成。兴奋性神经递质l-谷氨酸结合后,mGlus细胞外部分(VFT + CRD)的大构象变化诱导不对称TMD构型,激活G蛋白。这种不对称激活过程与其他C家族GPCRs具有共同的特征,如钙敏感受体和γ-氨基丁酸B受体。
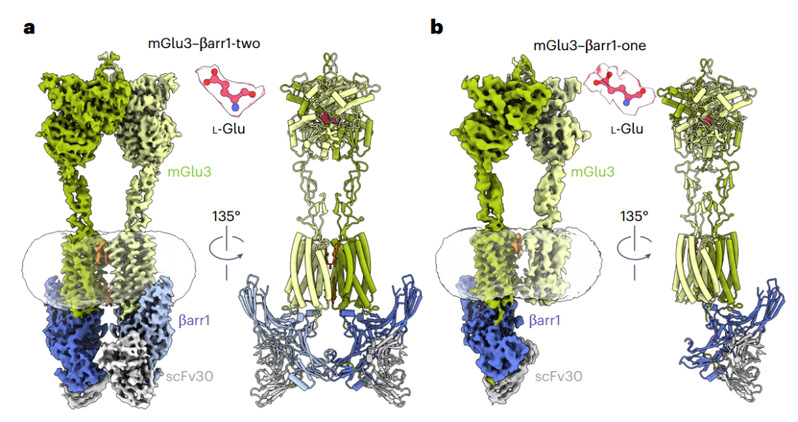
mGlu3–βarr 1复合物的整体结构(图源自Nature Chemical Biology)
该研究报道了与βarr1偶联的代谢型谷氨酸受体亚型3 (mGlu3)的两种结构,化学计量分别为2:1和2:2。l-谷氨酸结合的mGlu3二聚体处于非活性状态,两个捕蝇草结构域都关闭,不对称或对称地与βarr1结合。mGlu3原聚体的跨膜结构域通过由三个细胞内环和一个有序的C端区域形成的结合口袋与βarr1相互作用。mGlu3端尾部的三个磷酸化位点(pS857、pS859和pT860)与βarr1的N结构域接合。βarr1稳定无活性构象的mGlu3,以TM3/TM4–TM3/TM4二聚体界面为特征,以前在mGlu3的负变构调节剂结合结构中观察到。总之,mGlu3–βarr1复合物结构揭示了复合物组装、相互作用模式和构象状态转变的惊人方面,为βarr介导的C家族GPCRs失活提供了重要的见解。



